質粒存在于許多細菌以及酵母菌等生物中,是細胞染色體外能夠自主復制的很小的環狀DNA分子。在基因工程中,質粒制備可將質粒作為目的基因的載體,在新的宿主生物體中正常表達。質粒DNA可以作為疫苗或治療性藥物單獨使用,或在病毒載體生產中作為病毒包裝的原料。
質粒制備的步驟
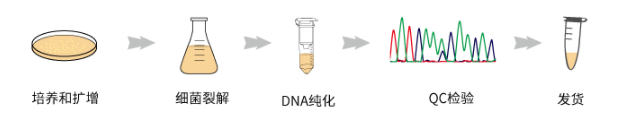
質粒制備流程圖
質粒制備常見問題
Q:轉化后克隆數量少
A:可以設置陰性和陽性對照。克隆過程中,陰性對照-空載長出菌落,判定可能是酶切不完全導致,陽性對照不出斑,可能是轉化實驗的操作出現問題。感受態細胞切勿反復凍融,且熱激時間一定要精準到秒,同時正確使用抗生素或其他篩選標記。
Q:菌落太多但假陽性率高,挑不到正確克隆
A:菌落PCR鑒定引物需跨區域設計,一條引物設計在載體上,另外一條在目標片段上。如此可避免假陽性克隆又篩除反向插入片段,還可以通過提取質粒酶切跑膠進一步排除錯誤克隆。
Q:大腸桿菌老化
A:建議涂布平板培養后,重新挑選新菌落進行液體培養。
Q:質粒未全部溶解
A:洗脫溶解質粒時,可適當加溫或延長溶解時間。
Q:質粒提取不成功
A:裂解時間過長,一般不應超過5分鐘。吸附時間,溶解時間不夠都會導致質粒DNA提取實驗失敗。
質粒制備|泓迅生物
泓迅生物擁有完善的質粒制備生產線,確保提供無RNA污染、無基因組污染的高質量無菌質粒,可將內毒素含量控制在較低水平(< 100EU/mg、<30EU/mg、<5EU/mg,供選擇)。另外我們還提供序列驗證、限制酶酶切和內毒素分析等服務,滿足各領域客戶多樣化的下游應用,如轉染、抗體制備,疫苗和基因治療研究等。
案例分享——轉染級質粒制備
將質粒轉化后挑取單克隆菌落進行培養,抽提菌液進行酶切及測序驗證,對符合要求的質粒進行大批量接菌抽提,之后對各批次抽提質粒進行酶切驗證,無誤后混合所有抽提質粒,最后對大抽質粒進行去內毒素處理,48h細菌檢測如圖1所示。
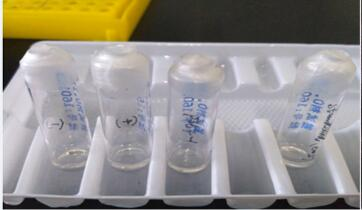
圖1 內毒素檢測
內毒素檢測結果為陰性對照不凝固,陽性對照凝固,測試稀釋樣品不凝固,標準品不凝固,證明去內毒素處理成功。
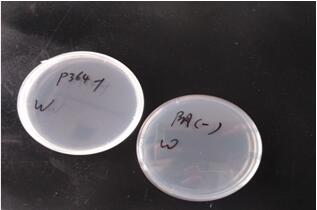
經過細菌檢測結果比對,48h無抗培養基均不長斑,通過無菌檢測。
 Syno?C 引物合成
Syno?C 引物合成 RNA合成
RNA合成 mRNA合成
mRNA合成 Syno?GS 基因合成
Syno?GS 基因合成 載體構建
載體構建 高通量及DNA文庫構建
高通量及DNA文庫構建 CRISPR基因編輯平臺
CRISPR基因編輯平臺 病毒包裝
病毒包裝 基因測序及分析
基因測序及分析 重組蛋白表達平臺
重組蛋白表達平臺 抗體工程平臺
抗體工程平臺 多肽服務
多肽服務 生物信息學分析與設計
生物信息學分析與設計 CRISPR文庫
CRISPR文庫 ProXpress蛋白快速檢測
ProXpress蛋白快速檢測 CRISPR 質粒
CRISPR 質粒





















